近日,醫(yī)學(xué)影像學(xué)院張輝教授團(tuán)隊(duì)在中科院Top 1區(qū)期刊《Acta Pharmaceutica Sinica B》(影響因子:7.097)上,發(fā)表了題為《Protease-triggered bioresponsive drug delivery for the targeted theranostics of malignancy》(蛋白酶響應(yīng)藥物遞釋體系用于惡性腫瘤靶向診療)的前沿綜述,高度總結(jié)蛋白酶的靶向策略并精準(zhǔn)分析其在癌癥診療中的應(yīng)用現(xiàn)狀和發(fā)展趨勢(shì)!
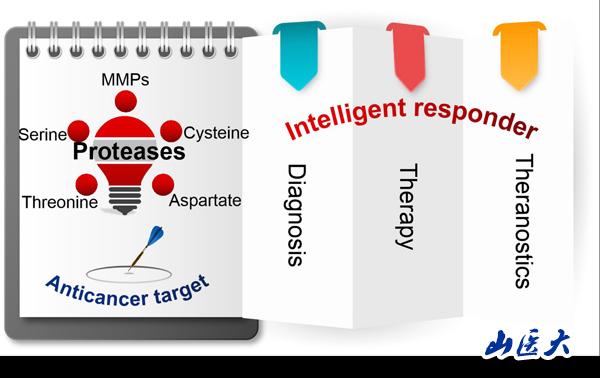
惡性腫瘤嚴(yán)重威脅人類(lèi)健康,在全球尤其是中國(guó)的發(fā)病率和死亡率逐年遞增。手術(shù)、化療和放療是臨床抗癌“三板斧”,但仍遭遇術(shù)前擴(kuò)散、病理復(fù)雜、副作用強(qiáng)、轉(zhuǎn)移耐藥等困擾。腫瘤微環(huán)境激勵(lì)的藥物遞釋是解決這些缺陷的有力方式。其中,蛋白酶特異性高,催化性強(qiáng),反應(yīng)溫和,在腫瘤中高表達(dá),使其不僅可作為檢測(cè)/預(yù)后標(biāo)志物和分子治療靶點(diǎn),還可在介導(dǎo)癌癥智能診療中彰顯奇效。
納米醫(yī)學(xué)的興起使得里程碑式的納米技術(shù)在高效呈遞并靶向輸運(yùn)生物活性物質(zhì)并用于癌癥管理中起到不可估量的推動(dòng)作用。結(jié)合蛋白酶的重要生理病理功能,一系列酶響應(yīng)多功能納米遞釋系統(tǒng)脫穎而出,在優(yōu)化藥物體內(nèi)分布、提高診斷敏感性、拓寬治療窗口、增強(qiáng)診療協(xié)同等方面突顯優(yōu)勢(shì),已成為引領(lǐng)醫(yī)藥學(xué)研究前沿的方向之一。
該研究在簡(jiǎn)述蛋白酶分類(lèi)及結(jié)構(gòu)功能基礎(chǔ)上,重點(diǎn)討論了蛋白酶觸發(fā)的多功能納米探針構(gòu)建及其在惡性腫瘤精準(zhǔn)診斷和靶向治療中應(yīng)用的最新進(jìn)展。另外,深入挖掘了納米復(fù)合物在體系設(shè)計(jì)、規(guī)模生產(chǎn)、潛在毒性及酶/底物匹配等方面的關(guān)鍵問(wèn)題。這一系統(tǒng)綜述和前沿分析為推動(dòng)蛋白酶響應(yīng)納米平臺(tái)在癌癥診療中應(yīng)用的臨床轉(zhuǎn)化提供了理論支撐和技術(shù)指引。
文章第一作者為醫(yī)學(xué)影像學(xué)院青年教師、博士后李亞楠,通訊作者為張輝教授和江西中醫(yī)藥大學(xué)孫勇兵副教授、西安交通大學(xué)安菲菲副教授,山西醫(yī)科大學(xué)為第一作者單位和通訊作者單位。上述成果得到國(guó)家自然科學(xué)基金、中國(guó)博士后科學(xué)基金等資助。
(圖文/李亞楠)






