近日,本團(tuán)隊單細(xì)胞多維分析領(lǐng)域取得重要進(jìn)展,相關(guān)研究以“Multiplex Profiling of Biomarker and Drug Uptake in Single Cells Using Microfluidic Flow Cytometry and Mass Spectrometry”為題發(fā)表在國際著名期刊《ACS Nano》上(中科院一區(qū)TOP,影響因子為17.1)。東北大學(xué)王建華教授、陳明麗教授和新加坡國立大學(xué)LimChweeTeck教授為共同通訊作者,第一作者為本團(tuán)隊青年教師張璇。
已有研究表明,腫瘤細(xì)胞表現(xiàn)出顯著的單細(xì)胞異質(zhì)性和標(biāo)志物多樣性,對其進(jìn)行多維度單細(xì)胞分析有助于精準(zhǔn)診斷和個性化治療。然而臨床樣本中腫瘤細(xì)胞樣品極為珍貴,通過傳統(tǒng)離心的手段有可能造成樣品損傷和丟失。
為解決上述問題,本工作開發(fā)了一種光譜-質(zhì)譜二維單細(xì)胞檢測策略,使用適配體標(biāo)記的高表面積生物功能化納米探針識別表達(dá)特異性蛋白的腫瘤細(xì)胞,利用集成了單細(xì)胞排列單元、樣品純化單元、熒光信號收集視窗的微流控芯片,對生物樣品中的目標(biāo)細(xì)胞進(jìn)行聚焦、排列、純化,借助激光誘導(dǎo)熒光(LIF)對6-FAM熒光基團(tuán)的高響應(yīng)信號和電感耦合等離子體質(zhì)譜(ICPMS)對195Pt的高靈敏度識別,用于在單細(xì)胞分辨率下在線分析單細(xì)胞上的鉑類藥物攝取和受影響的PTK7蛋白質(zhì)表達(dá)及其相關(guān)細(xì)胞表型分析。
與常規(guī)微流控螺旋通道相比,增強(qiáng)型螺旋單細(xì)胞聚焦單元可以在溫和流速下實(shí)現(xiàn)單細(xì)胞的高通量排列;更為簡潔的過濾純化單元可以省去傳統(tǒng)細(xì)胞樣品處理中冗余的離心清洗步驟,極大地節(jié)約樣品純化時間并避免不必要的樣品損失;依靠納米粒子本身巨大的表面積(1.16×105nm2)耦聯(lián)近3000條Sgc8適配體制成的高親和力適配體納米探針(Kd= 0.25 nM)可以識別樣品中的所有目標(biāo)細(xì)胞,這些標(biāo)記熒光基團(tuán)的適配體可以選擇性地與靶細(xì)胞上的PTK7蛋白結(jié)合,并通過狹長的信號收集視窗以被LIF采集對應(yīng)的單細(xì)胞熒光信號,進(jìn)而提供細(xì)胞中PTK7蛋白的表達(dá)情況;隨后引入ICPMS完成單細(xì)胞中奧沙利鉑(OXA)藥物的攝取情況定量分析。與傳統(tǒng)單細(xì)胞商用霧化器相比,本策略的單細(xì)胞測量效率提高近9倍(90.6%),這對測定稀有細(xì)胞樣品是極為重要的。此外,本方法采用水平進(jìn)樣方式,相較傳統(tǒng)微流控芯片垂直進(jìn)樣方式可以盡可能地降低接口處不必要的繞流現(xiàn)象,有利于保持本已排列好的單細(xì)胞穩(wěn)定地進(jìn)入檢測器,降低單個信號對應(yīng)多細(xì)胞事件的風(fēng)險。
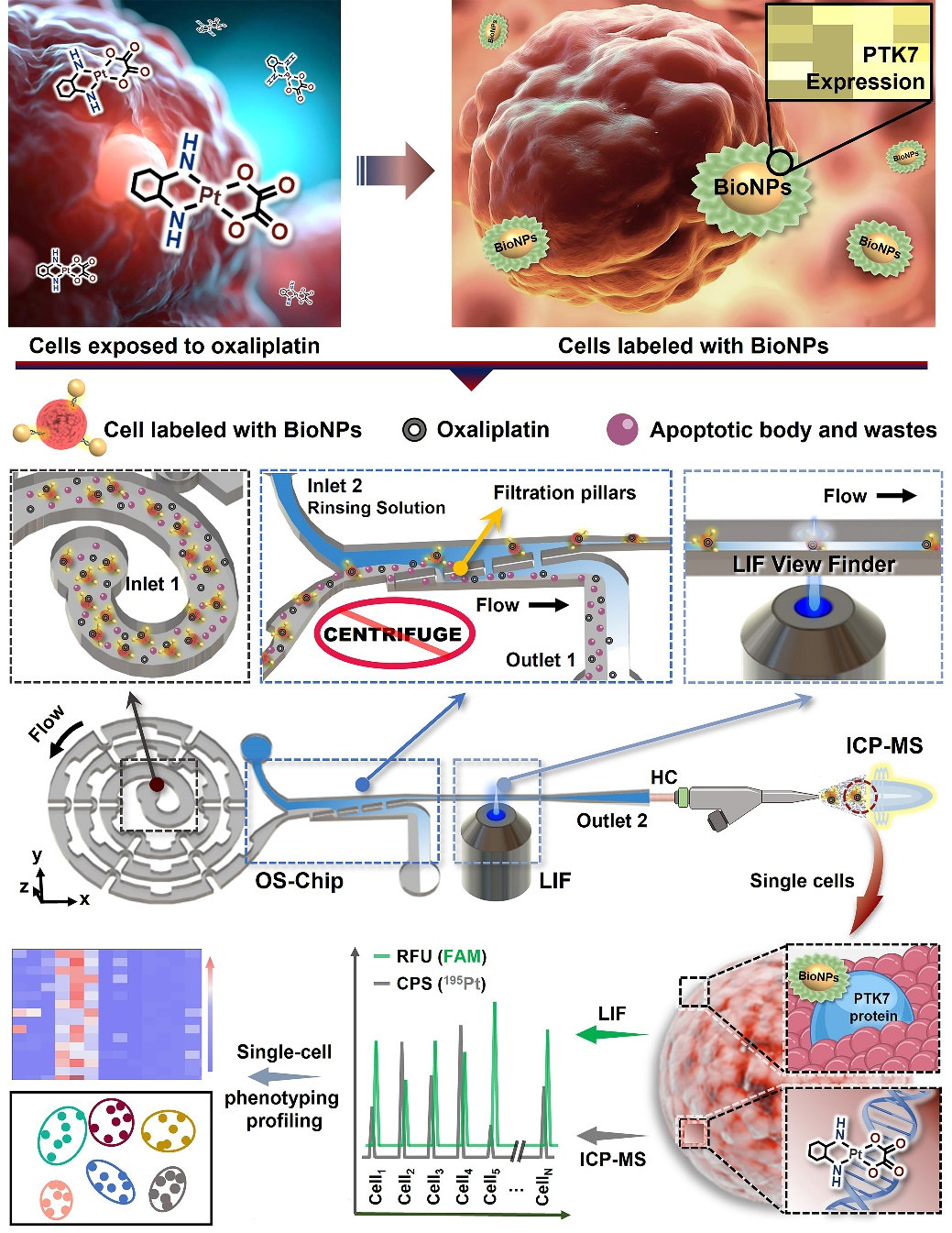
本系統(tǒng)進(jìn)行單細(xì)胞光譜/質(zhì)譜檢測的工作原理



