研究內(nèi)容簡介:
肝臟作為藥物代謝和解毒的主要器官,極易受到損傷,功能嚴重受損。因此,肝損傷的原位診斷和實時監(jiān)測具有重要意義,但由于缺乏可靠的無創(chuàng)體內(nèi)可視化方法,因此仍然受到限制。生理微環(huán)境在病理生理過程的早期就開始異常變化,并隨著其發(fā)展而不斷變化。粘度作為生理微環(huán)境的重要參數(shù),在肝損傷的過程中不可而避免地會發(fā)生變化,因此實時檢測肝臟損傷過程中的粘度變化對肝病的早期干預和治療具有重要意義。
聚集誘導發(fā)光(AIE)是唐本忠院士于2001年提出的一個光物理現(xiàn)象,是目前世界上為數(shù)不多的、由華人學者提出和引領(lǐng)的原創(chuàng)性概念之一。聚集誘導發(fā)光材料的開發(fā)被列為納米技術(shù)史上50個里程碑之一,以及支撐即將來臨的納米光革命的四大納米材料體系之一。AIE材料的發(fā)光機制也使其與粘度響應的發(fā)光增強目標不謀而合,該工作選擇聚集誘導發(fā)光探針,DPXBI,其可在近紅外第二窗口(NIR-II)發(fā)光,并用于肝損傷的早期診斷。
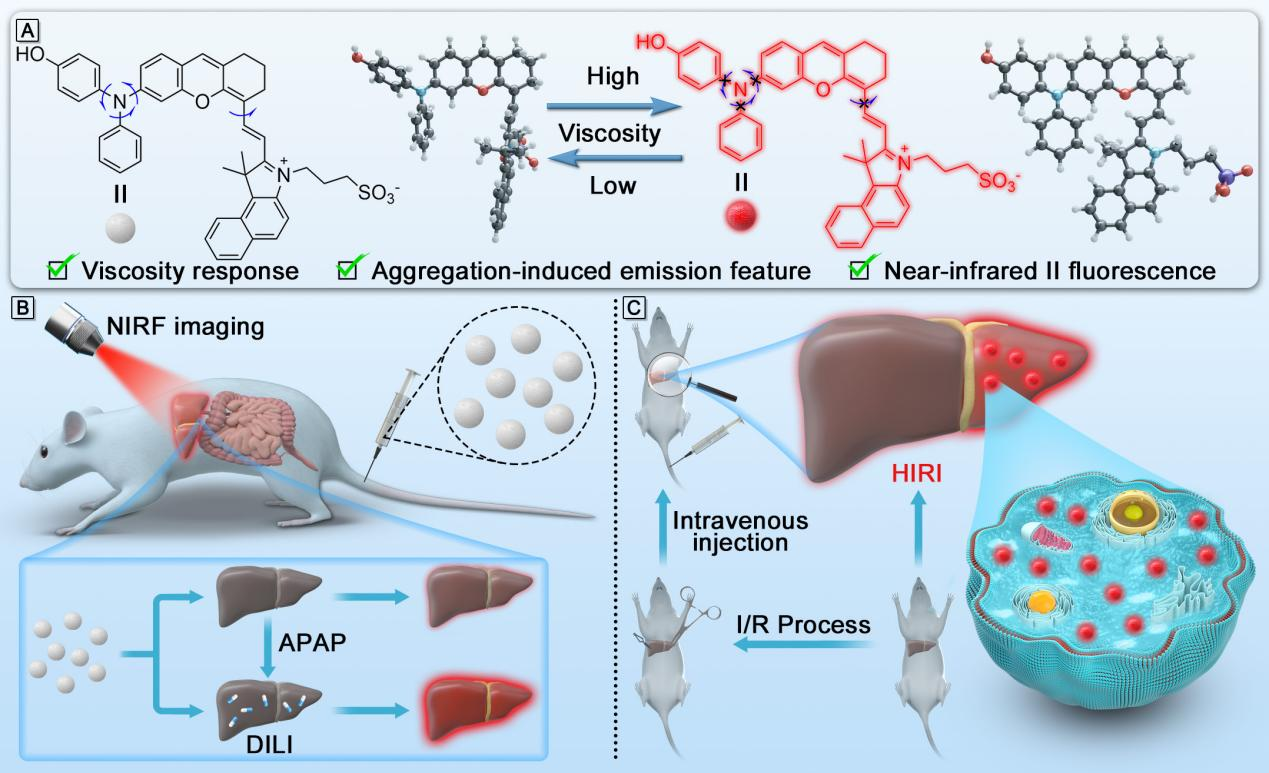
圖1.DPXBI分子和成像肝損傷示意圖
作者將電子受體(苯并吲哚磺酸鹽)與分子轉(zhuǎn)子二苯胺氧雜蒽通過乙烯橋連,構(gòu)建了高粘度敏感的AIEgen,即DPXBI。DPXBI具有良好的發(fā)光性能、優(yōu)異的水溶性、化學穩(wěn)定性強等特點,對粘度的波動非常敏感,可以通過NIR-II熒光強度變化展現(xiàn)快速響應和高選擇性。
DPXBI優(yōu)異的粘度響應能力使其能夠精準地監(jiān)測藥物誘導肝損傷(DILI)和肝缺血再灌注損傷(HIRI),具有高的圖像對比度。通過粘度檢測肝損傷的策略,實現(xiàn)了肝損傷的早期檢測,在小鼠模型檢測肝損傷可以比經(jīng)典的臨床檢測肝損傷至少早幾個小時。
當使用保肝藥物對DILI小鼠治療后,DPXBI能夠動態(tài)觀察到體內(nèi)肝臟治療后的改善過程。體內(nèi)的成像結(jié)果驗證了DPXBI具有較高的穩(wěn)定性和對粘度的敏感性,不受假陽性信號干擾。這些結(jié)果表明,DPXBI是研究粘度相關(guān)病理和生理過程的一種有力的工具。
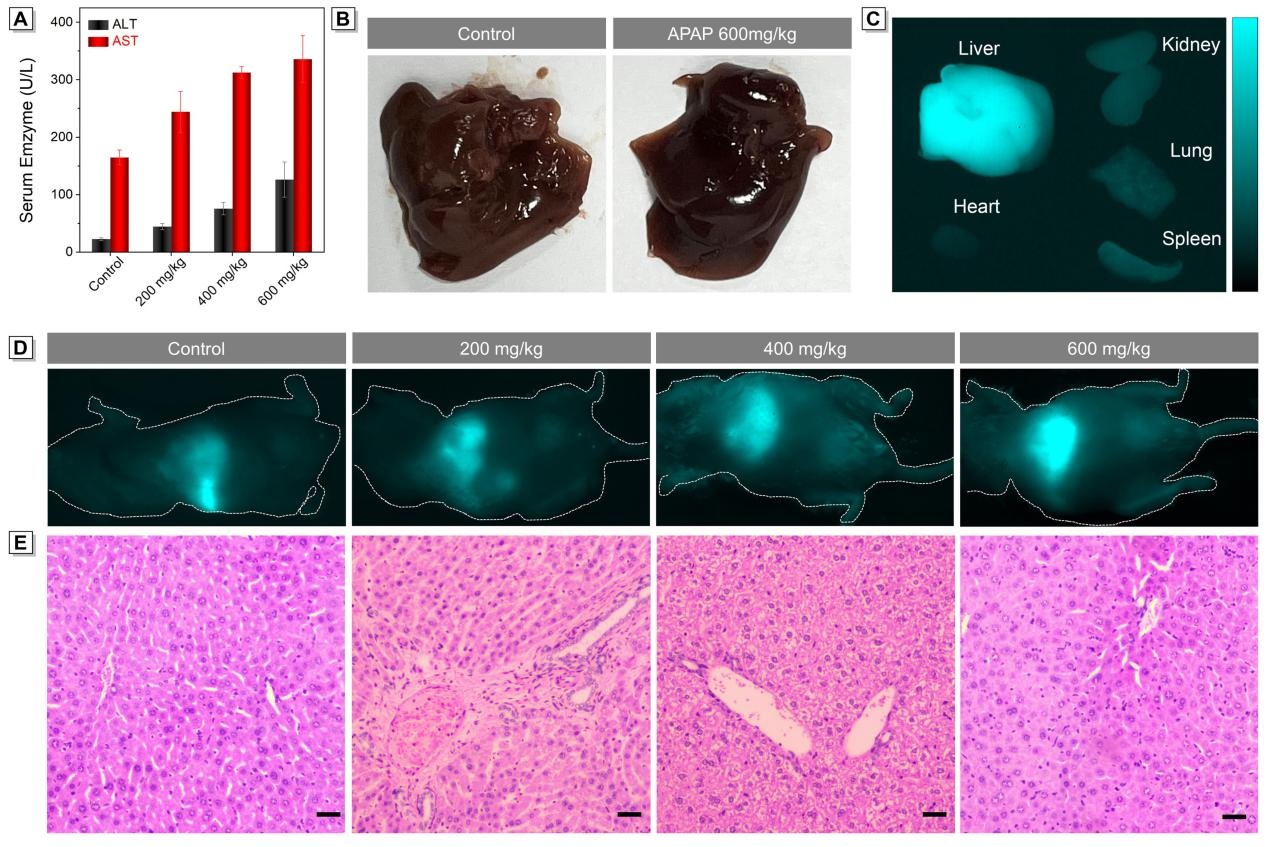
圖2.DILI模型小鼠的建立驗證和不同程度藥物誘導肝損傷小鼠體內(nèi)成像。
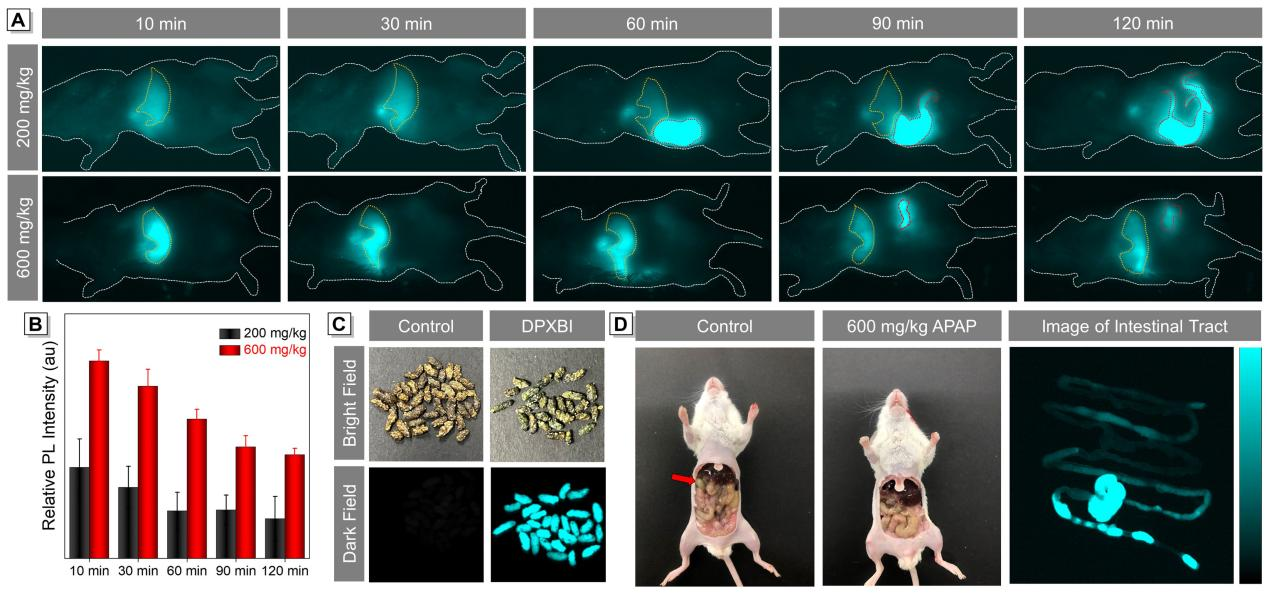
圖3.不同程度藥物誘導肝損傷小鼠代謝研究成像。
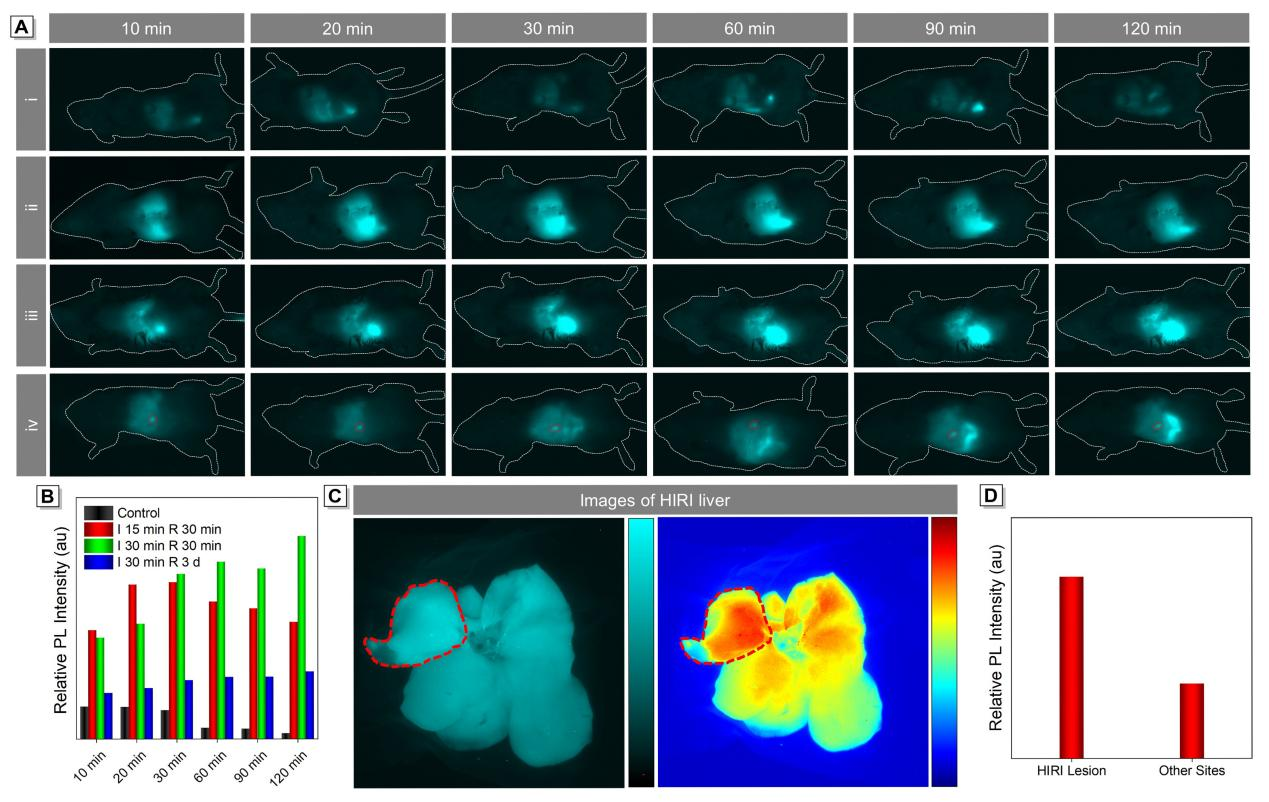
圖4.不同HIRI小鼠的實時NIR-Ⅱ熒光成像,通過粘度響應可以觀察到細微的損傷部位。



